आज पीआरपी के नाम से जानी जाने वाली अवधारणा पहली बार 1970 के दशक में हेमेटोलॉजी के क्षेत्र में सामने आई।हेमटोलॉजिस्ट ने दशकों पहले परिधीय रक्त में बेसल मूल्यों से ऊपर प्लेटलेट काउंट से प्राप्त प्लाज्मा का वर्णन करने के प्रयास में पीआरपी शब्द गढ़ा था।एक दशक से भी अधिक समय के बाद, पीआरपी का उपयोग मैक्सिलोफेशियल सर्जरी में प्लेटलेट-रिच फाइब्रिन (पीआरएफ) के रूप में किया गया था।इस पीआरपी व्युत्पन्न में फाइब्रिन सामग्री इसके चिपकने वाले और होमोस्टैटिक गुणों के लिए बहुत मूल्यवान है, जबकि पीआरपी में लगातार सूजन-रोधी गुण होते हैं और कोशिका प्रसार को उत्तेजित करते हैं।अंततः, 1990 के दशक के आसपास, पीआरपी लोकप्रिय हो गया, और अंततः, प्रौद्योगिकी को अन्य चिकित्सा क्षेत्रों में स्थानांतरित कर दिया गया।तब से, इस सकारात्मक जीव विज्ञान का बड़े पैमाने पर अध्ययन किया गया है और पेशेवर एथलीटों में विभिन्न मस्कुलोस्केलेटल चोटों के इलाज के लिए इसे लागू किया गया है, जिससे इसके व्यापक मीडिया का ध्यान आकर्षित हुआ है।आर्थोपेडिक्स और स्पोर्ट्स मेडिसिन में प्रभावी होने के अलावा, पीआरपी का उपयोग नेत्र विज्ञान, स्त्री रोग, मूत्रविज्ञान और कार्डियोलॉजी, बाल चिकित्सा और प्लास्टिक सर्जरी में किया जाता है।हाल के वर्षों में, पीआरपी की त्वचा विशेषज्ञों द्वारा त्वचा के अल्सर, निशान संशोधन, ऊतक पुनर्जनन, त्वचा कायाकल्प और यहां तक कि बालों के झड़ने का इलाज करने की क्षमता के लिए भी प्रशंसा की गई है।
इस तथ्य को ध्यान में रखते हुए कि पीआरपी सीधे उपचार और सूजन प्रक्रियाओं में हेरफेर करने के लिए जाना जाता है, उपचार कैस्केड को एक संदर्भ के रूप में पेश किया जाना चाहिए।उपचार प्रक्रिया को निम्नलिखित चार चरणों में विभाजित किया गया है: हेमोस्टेसिस;सूजन और जलन;सेलुलर और मैट्रिक्स प्रसार, और अंत में घाव रीमॉडलिंग।
1. ऊतक उपचार
एक ऊतक-उपचार कैस्केड सक्रिय होता है, एक प्रक्रिया जो प्लेटलेट एकत्रीकरण, थक्का गठन और एक अस्थायी बाह्य मैट्रिक्स (ईसीएम) के विकास की ओर ले जाती है। प्लेटलेट्स फिर उजागर कोलेजन और ईसीएम प्रोटीन का पालन करते हैं, जिससे रिलीज में α-ग्रैन्यूल्स की उपस्थिति शुरू हो जाती है। बायोएक्टिव अणु। प्लेटलेट्स में विभिन्न प्रकार के बायोएक्टिव अणु होते हैं, जिनमें वृद्धि कारक, केमोकाइन और साइटोकिन्स, साथ ही प्रोस्टाग्लैंडिंस, प्रोस्टेटिक साइक्लिन, हिस्टामाइन, थ्रोम्बोक्सेन, सेरोटोनिन और ब्रैडीकाइनिन जैसे सूजन-रोधी मध्यस्थ शामिल हैं।
उपचार प्रक्रिया का अंतिम चरण घाव के पुनर्निर्माण पर निर्भर करता है।एनाबॉलिक और कैटोबोलिक प्रतिक्रियाओं के बीच संतुलन स्थापित करने के लिए ऊतक रीमॉडलिंग को सख्ती से विनियमित किया जाता है।इस चरण के दौरान, प्लेटलेट-व्युत्पन्न वृद्धि कारक (पीडीजीएफ), परिवर्तनकारी वृद्धि कारक (टीजीएफ-β) और फ़ाइब्रोनेक्टिन फ़ाइब्रोब्लास्ट के प्रसार और प्रवासन के साथ-साथ ईसीएम घटकों के संश्लेषण को उत्तेजित करते हैं।हालाँकि, घाव के पकने का समय काफी हद तक घाव की गंभीरता, व्यक्तिगत विशेषताओं और घायल ऊतक की विशिष्ट उपचार क्षमता पर निर्भर करता है, और कुछ पैथोफिजियोलॉजिकल और चयापचय कारक उपचार प्रक्रिया को प्रभावित कर सकते हैं, जैसे ऊतक इस्किमिया, हाइपोक्सिया, संक्रमण , विकास कारक असंतुलन, और यहां तक कि चयापचय सिंड्रोम से संबंधित रोग भी।
एक प्रो-इंफ्लेमेटरी माइक्रोएन्वायरमेंट जो उपचार प्रक्रिया में हस्तक्षेप करता है।मामले को जटिल बनाने के लिए, उच्च प्रोटीज गतिविधि भी है जो विकास कारक (जीएफ) की प्राकृतिक क्रिया को रोकती है।माइटोजेनिक, एंजियोजेनिक और केमोटैक्टिक गुणों के अलावा, पीआरपी कई विकास कारकों, बायोमोलेक्यूल्स का भी एक समृद्ध स्रोत है जो बढ़ी हुई सूजन को नियंत्रित करके और एनाबॉलिक उत्तेजनाओं को स्थापित करके सूजन वाले ऊतकों में हानिकारक प्रभावों का प्रतिकार कर सकता है।इन गुणों को देखते हुए, शोधकर्ताओं को विभिन्न प्रकार की जटिल चोटों के इलाज में काफी संभावनाएं मिल सकती हैं।
2. साइटोकाइन
पीआरपी में मौजूद साइटोकिन्स ऊतक मरम्मत प्रक्रियाओं में हेरफेर करने और सूजन संबंधी क्षति को नियंत्रित करने में महत्वपूर्ण भूमिका निभाते हैं।एंटी-इंफ्लेमेटरी साइटोकिन्स जैव रासायनिक अणुओं का एक व्यापक स्पेक्ट्रम है जो प्रो-इंफ्लेमेटरी साइटोकिन प्रतिक्रियाओं में मध्यस्थता करता है, जो मुख्य रूप से सक्रिय मैक्रोफेज द्वारा प्रेरित होता है।सूजनरोधी साइटोकिन्स सूजन को नियंत्रित करने के लिए विशिष्ट साइटोकिन अवरोधकों और घुलनशील साइटोकिन रिसेप्टर्स के साथ बातचीत करते हैं।इंटरल्यूकिन (IL)-1 रिसेप्टर विरोधी, IL-4, IL-10, IL-11 और IL-13 को मुख्य सूजनरोधी साइटोकिन्स के रूप में वर्गीकृत किया गया है।घाव के प्रकार के आधार पर, कुछ साइटोकिन्स, जैसे इंटरफेरॉन, ल्यूकेमिया निरोधात्मक कारक, टीजीएफ-β और आईएल-6, प्रो- या विरोधी भड़काऊ प्रभाव प्रदर्शित कर सकते हैं।TNF-α, IL1 और IL-18 में कुछ साइटोकिन रिसेप्टर्स होते हैं जो अन्य प्रोटीनों के प्रो-इंफ्लेमेटरी प्रभाव को रोक सकते हैं [37]।IL-10 सबसे शक्तिशाली एंटी-इंफ्लेमेटरी साइटोकिन्स में से एक है, यह IL-1, IL-6 और TNF-α जैसे प्रो-इंफ्लेमेटरी साइटोकिन्स को डाउन-रेगुलेट कर सकता है और एंटी-इंफ्लेमेटरी साइटोकिन्स को अप-रेगुलेट कर सकता है।ये प्रति-नियामक तंत्र प्रो-इंफ्लेमेटरी साइटोकिन्स के उत्पादन और कार्य में महत्वपूर्ण भूमिका निभाते हैं।इसके अलावा, कुछ साइटोकिन्स विशिष्ट सिग्नलिंग प्रतिक्रियाओं को ट्रिगर कर सकते हैं जो फ़ाइब्रोब्लास्ट को उत्तेजित करते हैं, जो ऊतक की मरम्मत के लिए महत्वपूर्ण हैं।सूजन संबंधी साइटोकिन्स TGFβ1, IL-1β, IL-6, IL-13 और IL-33 फाइब्रोब्लास्ट को मायोफाइब्रोब्लास्ट में अंतर करने और ECM में सुधार करने के लिए उत्तेजित करते हैं [38]।बदले में, फ़ाइब्रोब्लास्ट साइटोकिन्स TGF-β, IL-1β, IL-33, CXC, और CC केमोकाइन का स्राव करते हैं, जो मैक्रोफेज जैसी प्रतिरक्षा कोशिकाओं को सक्रिय और भर्ती करके प्रो-इंफ्लेमेटरी प्रतिक्रियाओं को बढ़ावा देते हैं।घाव स्थल पर इन सूजन कोशिकाओं की कई भूमिकाएँ होती हैं, मुख्य रूप से घाव साफ़ करने को बढ़ावा देना - साथ ही केमोकाइन, मेटाबोलाइट्स और विकास कारकों के जैवसंश्लेषण को बढ़ावा देना, जो नए ऊतकों के पुनर्निर्माण के लिए आवश्यक हैं।इस प्रकार, पीआरपी में मौजूद साइटोकिन्स कोशिका प्रकार-मध्यस्थ प्रतिरक्षा प्रतिक्रियाओं को उत्तेजित करने, सूजन चरण के समाधान को चलाने में महत्वपूर्ण भूमिका निभाते हैं।वास्तव में, कुछ शोधकर्ताओं ने इस प्रक्रिया को "पुनर्योजी सूजन" का नाम दिया है, यह सुझाव देते हुए कि सूजन का चरण, रोगी की बेचैनी के बावजूद, एक सफल निष्कर्ष तक पहुंचने के लिए ऊतक की मरम्मत प्रक्रिया के लिए एक महत्वपूर्ण कदम है, एपिजेनेटिक तंत्र को देखते हुए जिसके द्वारा सूजन के संकेत सेलुलर को बढ़ावा देते हैं प्लास्टिसिटी
3. फाइब्रिन
प्लेटलेट्स में फाइब्रिनोलिटिक प्रणाली से संबंधित कई कारक होते हैं जो फाइब्रिनोलिटिक प्रतिक्रिया को बढ़ा या घटा सकते हैं।थक्का क्षरण में हेमेटोलॉजिकल घटकों और प्लेटलेट फ़ंक्शन का अस्थायी संबंध और सापेक्ष योगदान समुदाय में व्यापक चर्चा के योग्य मुद्दा बना हुआ है।साहित्य केवल प्लेटलेट्स पर ध्यान केंद्रित करने वाले कई अध्ययन प्रस्तुत करता है, जो उपचार प्रक्रिया को प्रभावित करने की अपनी क्षमता के लिए जाने जाते हैं।कई उत्कृष्ट अध्ययनों के बावजूद, अन्य हेमटोलॉजिकल घटक, जैसे जमावट कारक और फाइब्रिनोलिटिक प्रणाली, भी प्रभावी घाव की मरम्मत में महत्वपूर्ण योगदान देते पाए गए हैं।परिभाषा के अनुसार, फाइब्रिनोलिसिस एक जटिल जैविक प्रक्रिया है जो फाइब्रिन के क्षरण को सुविधाजनक बनाने के लिए कुछ एंजाइमों की सक्रियता पर निर्भर करती है।फाइब्रिनोलिटिक प्रतिक्रिया का सुझाव अन्य लेखकों द्वारा दिया गया है कि फाइब्रिन क्षरण उत्पाद (एफडीपी) वास्तव में आणविक एजेंट हो सकते हैं जो ऊतक की मरम्मत को उत्तेजित करने के लिए ज़िम्मेदार हैं, फाइब्रिन जमाव से पहले महत्वपूर्ण जैविक घटनाओं का अनुक्रम और एंजियोजेनेसिस से हटाने, जो घाव भरने के लिए आवश्यक है।चोट के बाद थक्के का बनना एक सुरक्षात्मक परत के रूप में कार्य करता है जो ऊतकों को रक्त की हानि, माइक्रोबियल एजेंटों के आक्रमण से बचाता है, और एक अस्थायी मैट्रिक्स भी प्रदान करता है जिसके माध्यम से कोशिकाएं मरम्मत के दौरान स्थानांतरित हो सकती हैं।यह थक्का क्रॉस-लिंक्ड फाइब्रिन फाइब्रस नेटवर्क में सेरीन प्रोटीज और प्लेटलेट्स समुच्चय द्वारा फाइब्रिनोजेन के टूटने के कारण होता है।यह प्रतिक्रिया फाइब्रिन मोनोमर्स के पोलीमराइजेशन की शुरुआत करती है, जो रक्त के थक्के बनने की मुख्य घटना है।थक्के साइटोकिन्स और वृद्धि कारकों के लिए भंडार के रूप में भी कार्य कर सकते हैं, जो सक्रिय प्लेटलेट्स के क्षरण पर निकलते हैं।फाइब्रिनोलिटिक प्रणाली को प्लास्मिन द्वारा कसकर नियंत्रित किया जाता है और कोशिका प्रवास, विकास कारक जैवउपलब्धता और ऊतक सूजन और पुनर्जनन में शामिल अन्य प्रोटीज प्रणालियों के विनियमन को बढ़ावा देने में महत्वपूर्ण भूमिका निभाता है।फाइब्रिनोलिसिस में प्रमुख घटक, जैसे यूरोकाइनेज प्लास्मिनोजेन एक्टिवेटर रिसेप्टर (यूपीएआर) और प्लास्मिनोजेन एक्टिवेटर इनहिबिटर -1 (पीएआई-1) को मेसेनकाइमल स्टेम सेल (एमएससी) में व्यक्त किया जाता है, जो सफल घाव भरने के लिए आवश्यक एक विशेष सेल प्रकार है।
4. सेल माइग्रेशन
यूपीए-यूपीएआर एसोसिएशन के माध्यम से प्लास्मिनोजेन का सक्रियण एक ऐसी प्रक्रिया है जो सूजन कोशिका प्रवासन को बढ़ावा देती है क्योंकि यह बाह्य कोशिकीय प्रोटियोलिसिस को बढ़ाती है।चूंकि यूपीएआर में ट्रांसमेम्ब्रेन और इंट्रासेल्युलर डोमेन का अभाव है, इसलिए प्रोटीन को सेल माइग्रेशन को विनियमित करने के लिए इंटीग्रिन और विट्रेइन जैसे सह-रिसेप्टर्स की आवश्यकता होती है।इसके अलावा, यूपीए-यूपीएआर बाइंडिंग के परिणामस्वरूप विट्रीस कॉन्नेक्सिन और इंटीग्रिन के लिए यूपीएआर की आत्मीयता में वृद्धि हुई, जिससे कोशिका आसंजन को बढ़ावा मिला।प्लास्मिनोजेन एक्टीवेटर इनहिबिटर-1 (पीएआई-1) बदले में कोशिकाओं को अलग कर देता है, अपर-विट्रिन और इंटीग्रिन को नष्ट कर देता है- जब यह कोशिका की सतह पर यूपीए-अपर-इंटीग्रिन कॉम्प्लेक्स के यूपीए से जुड़ जाता है, ग्लास वोक्सल्स की परस्पर क्रिया।
पुनर्योजी चिकित्सा के संदर्भ में, मेसेनकाइमल स्टेम कोशिकाएं गंभीर अंग क्षति के संदर्भ में अस्थि मज्जा से जुटाई जाती हैं और इस प्रकार कई फ्रैक्चर वाले रोगियों के परिसंचरण में पाई जा सकती हैं।हालाँकि, कुछ परिस्थितियों में, जैसे अंतिम चरण की गुर्दे की विफलता, अंतिम चरण की यकृत विफलता, या हृदय प्रत्यारोपण के बाद अस्वीकृति की शुरुआत के दौरान, इन कोशिकाओं का रक्त में पता नहीं लगाया जा सकता है [66]।दिलचस्प बात यह है कि इन मानव अस्थि मज्जा-व्युत्पन्न मेसेनकाइमल (स्ट्रोमल) पूर्वज कोशिकाओं को स्वस्थ व्यक्तियों के रक्त में नहीं पाया जा सकता है [67]।अस्थि मज्जा मेसेनकाइमल स्टेम सेल जुटाव में यूपीएआर की भूमिका पहले भी प्रस्तावित की गई है, जो हेमेटोपोएटिक स्टेम सेल (एचएससी) जुटाव में होती है।वरबानेनी एट अल.परिणामों से पता चला कि यूपीएआर की कमी वाले चूहों में ग्रैनुलोसाइट कॉलोनी-उत्तेजक कारक के उपयोग ने एमएससी की विफलता का कारण बना, सेल प्रवास में फाइब्रिनोलिटिक प्रणाली की सहायक भूमिका को फिर से मजबूत किया।आगे के अध्ययनों से यह भी पता चला है कि ग्लाइकोसिफलोस्फेटिडिलिनोसिटॉल-एंकरयुक्त यूपीए रिसेप्टर्स कुछ इंट्रासेल्युलर सिग्नलिंग मार्गों को सक्रिय करके आसंजन, प्रवासन, प्रसार और भेदभाव को नियंत्रित करते हैं, इस प्रकार: प्रो-सर्वाइवल फॉस्फेटिडिलिनोसिटॉल 4,5-बिस्फोस्फेट 3-किनेज/एक्ट और ईआरके1/2 सिग्नलिंग मार्ग , और आसंजन काइनेज (एफएके)।
एमएससी ने घाव भरने के संदर्भ में और अधिक महत्व प्रदर्शित किया है।उदाहरण के लिए, प्लास्मिनोजेन की कमी वाले चूहों ने घाव भरने की घटनाओं में गंभीर देरी प्रदर्शित की, जिससे पता चलता है कि प्लास्मिन इस प्रक्रिया में गंभीर रूप से शामिल है।मनुष्यों में, प्लास्मिन की हानि से घाव भरने की जटिलताएँ भी हो सकती हैं।रक्त प्रवाह में व्यवधान ऊतक पुनर्जनन को महत्वपूर्ण रूप से बाधित कर सकता है, जो बताता है कि मधुमेह के रोगियों में ये पुनर्योजी प्रक्रियाएं अधिक चुनौतीपूर्ण क्यों हैं।
5. मोनोसाइट्स और पुनर्जनन प्रणाली
साहित्य के अनुसार, घाव भरने में मोनोसाइट्स की भूमिका के बारे में बहुत चर्चा होती है।मैक्रोफेज मुख्य रूप से रक्त मोनोसाइट्स से प्राप्त होते हैं और पुनर्योजी चिकित्सा में महत्वपूर्ण भूमिका निभाते हैं [81]।चूँकि न्यूट्रोफिल IL-4, IL-1, IL-6 और TNF-[अल्फा] का स्राव करते हैं, ये कोशिकाएँ आमतौर पर चोट लगने के लगभग 24-48 घंटे बाद घाव वाली जगह में प्रवेश करती हैं।प्लेटलेट्स थ्रोम्बिन और प्लेटलेट फैक्टर 4 (पीएफ4) जारी करते हैं, दो केमोकाइन जो मोनोसाइट्स की भर्ती और मैक्रोफेज और डेंड्राइटिक कोशिकाओं में उनके भेदभाव को बढ़ावा देते हैं।मैक्रोफेज की एक उल्लेखनीय विशेषता उनकी प्लास्टिसिटी है, यानी, फेनोटाइप को स्विच करने और एंडोथेलियल कोशिकाओं जैसे अन्य सेल प्रकारों में ट्रांसडिफरेंशियल करने की उनकी क्षमता, जो बाद में घाव माइक्रोएन्वायरमेंट में विभिन्न जैव रासायनिक उत्तेजनाओं के जवाब में विभिन्न कार्यों को प्रदर्शित करती है।सूजन कोशिकाएं दो प्रमुख फेनोटाइप, एम1 या एम2 को व्यक्त करती हैं, जो स्थानीय आणविक संकेत पर निर्भर करता है जो उत्तेजना का स्रोत है।एम1 मैक्रोफेज माइक्रोबियल एजेंटों से प्रेरित होते हैं और इस प्रकार इनका सूजन-रोधी प्रभाव अधिक होता है।इसके विपरीत, एम2 मैक्रोफेज आमतौर पर टाइप 2 प्रतिक्रिया से उत्पन्न होते हैं और इनमें सूजन-रोधी गुण होते हैं, जो आमतौर पर आईएल-4, आईएल-5, आईएल-9 और आईएल-13 में वृद्धि की विशेषता होती है।यह वृद्धि कारकों के उत्पादन के माध्यम से ऊतक की मरम्मत में भी शामिल है।एम1 से एम2 आइसोफॉर्म में संक्रमण काफी हद तक घाव भरने के बाद के चरणों से प्रेरित होता है, जहां एम1 मैक्रोफेज न्यूट्रोफिल एपोप्टोसिस को ट्रिगर करते हैं और इन कोशिकाओं की निकासी शुरू करते हैं)।न्यूट्रोफिल द्वारा फागोसाइटोसिस घटनाओं की एक श्रृंखला को सक्रिय करता है जिसमें साइटोकिन उत्पादन बंद हो जाता है, मैक्रोफेज का ध्रुवीकरण होता है और टीजीएफ-β1 जारी होता है।यह वृद्धि कारक मायोफाइब्रोब्लास्ट विभेदन और घाव संकुचन का एक प्रमुख नियामक है, जो सूजन के समाधान और हीलिंग कैस्केड में प्रसार चरण की शुरुआत की अनुमति देता है [57]।सेलुलर प्रक्रियाओं में शामिल एक अन्य अत्यधिक संबंधित प्रोटीन सेरीन (एसजी) है।यह हेमटोपोइएटिक कोशिका-स्रावित ग्रैनुलान विशिष्ट प्रतिरक्षा कोशिकाओं, जैसे मस्तूल कोशिकाओं, न्यूट्रोफिल और साइटोटॉक्सिक टी लिम्फोसाइट्स में स्रावित प्रोटीन के भंडारण के लिए आवश्यक पाया गया है।जबकि कई गैर-हेमेटोपोएटिक कोशिकाएं भी सेरोटोनिन को संश्लेषित करती हैं, सभी सूजन कोशिकाएं बड़ी मात्रा में इस प्रोटीन का उत्पादन करती हैं और इसे प्रोटीज़, साइटोकिन्स, केमोकाइन और विकास कारक सहित अन्य सूजन मध्यस्थों के साथ आगे की बातचीत के लिए कणिकाओं में संग्रहीत करती हैं।एसजी में नकारात्मक रूप से चार्ज किए गए ग्लाइकोसामिनोग्लाइकन (जीएजी) श्रृंखलाएं स्रावी ग्रेन्युल होमियोस्टेसिस के लिए महत्वपूर्ण प्रतीत होती हैं, क्योंकि वे सेल-, प्रोटीन- और जीएजी श्रृंखला-विशिष्ट तरीके से पर्याप्त रूप से चार्ज किए गए ग्रेन्युल घटकों के भंडारण को बांध और सुविधाजनक बना सकते हैं।पीआरपी में उनकी भागीदारी के संबंध में, वूल्फे और सहकर्मियों ने पहले दिखाया है कि एसजी की कमी दृढ़ता से परिवर्तित प्लेटलेट आकारिकी से जुड़ी हुई है;प्लेटलेट फैक्टर 4, बीटा-थ्रोमग्लोबुलिन और प्लेटलेट्स में पीडीजीएफ भंडारण में दोष;इन विट्रो में खराब प्लेटलेट एकत्रीकरण और स्राव और विवो रूप में घनास्त्रता दोष।इसलिए शोधकर्ताओं ने निष्कर्ष निकाला कि यह प्रोटीयोग्लाइकन घनास्त्रता का एक मुख्य नियामक प्रतीत होता है।
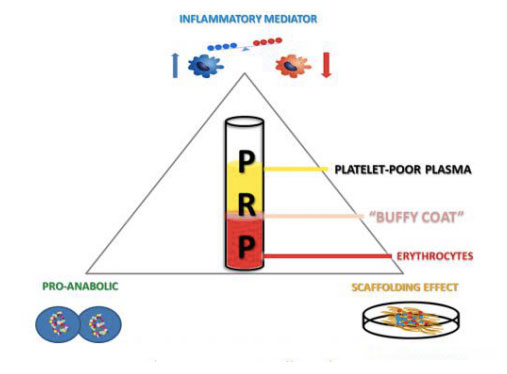
प्लेटलेट-समृद्ध उत्पाद किसी व्यक्ति के पूरे रक्त को इकट्ठा करके और सेंट्रीफ्यूज करके, मिश्रण को प्लाज्मा, प्लेटलेट्स, ल्यूकोसाइट्स और ल्यूकोसाइट्स वाली विभिन्न परतों में अलग करके प्राप्त किया जा सकता है।जब प्लेटलेट सांद्रता बेसल मूल्यों से अधिक होती है, तो न्यूनतम दुष्प्रभाव के साथ हड्डी और नरम ऊतकों का विकास तेज हो सकता है।ऑटोलॉगस पीआरपी उत्पादों का अनुप्रयोग एक अपेक्षाकृत नई जैव प्रौद्योगिकी है जो विभिन्न ऊतक चोटों की उत्तेजना और बेहतर उपचार में आशाजनक परिणाम दिखाता रहता है।इस वैकल्पिक चिकित्सीय दृष्टिकोण की प्रभावकारिता को विकास कारकों और प्रोटीन की एक विस्तृत श्रृंखला के सामयिक वितरण के लिए जिम्मेदार ठहराया जा सकता है, जो शारीरिक घाव भरने और ऊतक मरम्मत प्रक्रियाओं की नकल और समर्थन करता है।इसके अलावा, फाइब्रिनोलिटिक प्रणाली का समग्र ऊतक मरम्मत पर स्पष्ट रूप से महत्वपूर्ण प्रभाव पड़ता है।सूजन कोशिकाओं और मेसेनकाइमल स्टेम कोशिकाओं की सेलुलर भर्ती को बदलने की अपनी क्षमता के अलावा, यह घाव भरने वाले क्षेत्रों में और हड्डी, उपास्थि और मांसपेशियों सहित मेसोडर्मल ऊतकों के पुनर्जनन के दौरान प्रोटियोलिटिक गतिविधि को नियंत्रित करता है, और इसलिए मस्कुलोस्केलेटल दवा घटक में महत्वपूर्ण है।
चिकित्सा क्षेत्र में कई पेशेवरों द्वारा उपचार में तेजी लाना एक अत्यधिक मांग वाला लक्ष्य है, और पीआरपी एक सकारात्मक जैविक उपकरण का प्रतिनिधित्व करता है जो पुनर्योजी घटनाओं की उत्तेजना और अच्छी तरह से समन्वित अग्रानुक्रम में आशाजनक विकास की पेशकश करता रहता है।हालाँकि, चूंकि यह चिकित्सीय उपकरण जटिल बना हुआ है, खासकर जब से यह असंख्य बायोएक्टिव कारकों और उनके विभिन्न इंटरैक्शन तंत्रों और सिग्नलिंग प्रभावों को जारी करता है, आगे के अध्ययन की आवश्यकता है।
(इस लेख की सामग्री पुनर्मुद्रित है, और हम इस लेख में निहित सामग्री की सटीकता, विश्वसनीयता या पूर्णता के लिए कोई व्यक्त या निहित गारंटी नहीं देते हैं, और इस लेख की राय के लिए ज़िम्मेदार नहीं हैं, कृपया समझें।)
पोस्ट करने का समय: जुलाई-19-2022